為全面落實藥品安全專項整治工作部署,進一步加強新冠病毒檢測試劑產品質量安全監管,確保產品質量安全,有效服務疫情防控大局,國家藥監局發布最新通知,有以下七點要求:
1.持續從嚴從細抓好產品質量監管;
2.持續加強產品研制環節質量監管;
3.持續加強產品生產環節質量監管;
4.持續加強產品經營環節質量監管;
5.持續加強使用環節產品質量監管;
6.持續加強產品質量監督抽檢;
7.持續嚴厲打擊違法違規行為。
相較于三月發的做好新冠病毒抗原檢測試劑質量安全監管工作的通知,從最開始的加強注冊相關管理工作、加強生產環節監督檢查、加強經營環節監督檢查、嚴厲打擊違法違規行為,到現在的七大要求,雖說只多了三個要求,但是可以看出國家藥監局對于新冠病毒檢測試紙的重視程度、嚴抓程度,從源頭保證檢測試劑的安全。
新冠病毒檢測試劑是新冠肺炎疫情防控所需的重要產品。疫情暴發以來,國家藥監局持續加強新冠病毒檢測試劑質量安全監管,有力推動了企業主體責任和屬地監管責任的落實,有效強化了產品質量安全保障。新冠病毒檢測試劑屬于醫療器械類產品,首先從注冊審批上市環節就要做好嚴格把關,因此,相關醫療器械在國家藥品監督管理局的注冊審批流程上,一直被作為嚴格管控對象。
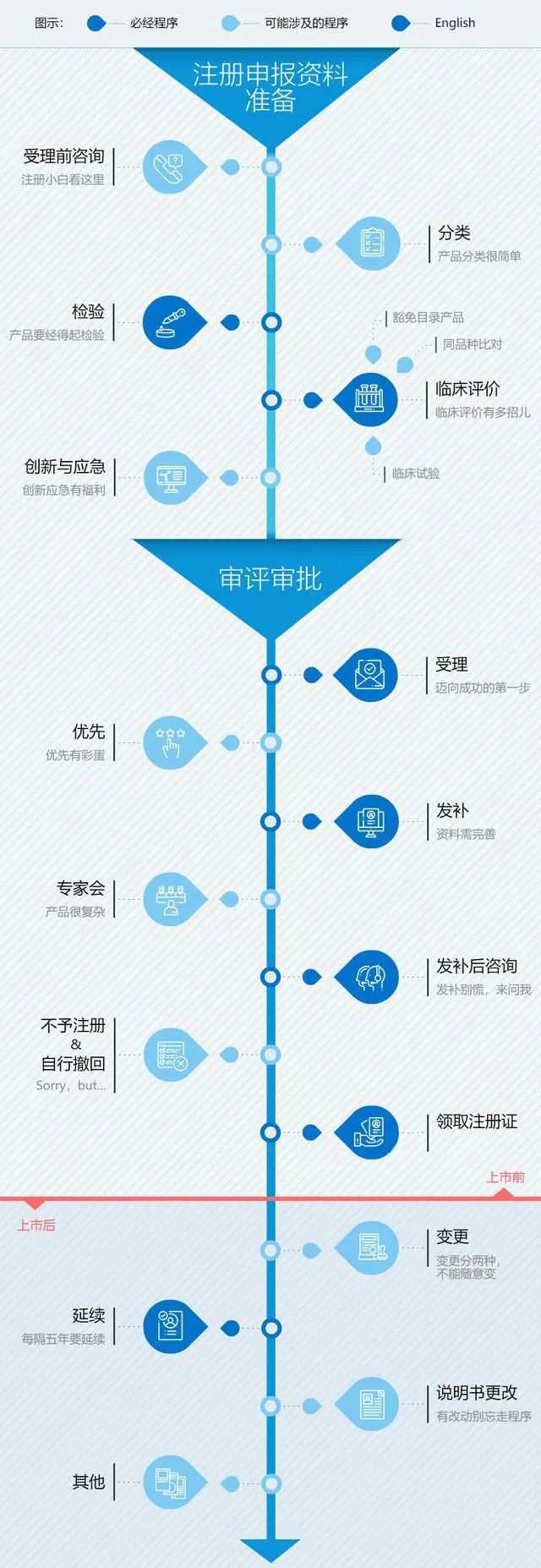
醫療器械在上市銷售之前,都需要到藥監局進行注冊備案,因為這樣對使用的醫療器械的安全性、有效性進行系統評價,以決定是否同意其銷售、使用。它分為境內醫療器械注冊和境外醫療器械注冊,境外的醫療器械不管是一類、二類、三類都要到北京國家食品藥品監督局辦理:境內的一、二類醫療器械在當地的省或市食品藥品監督局辦理,三類的到國家食品藥品監督局辦理。醫療器械注冊證是指醫療器械產品的合法身份證。
譯國譯民集團作為擁有近20年醫學翻譯經驗的服務商,為多個知名醫療器械企業提供新品上市注冊審批翻譯服務,熟知注冊審批流程,醫學翻譯經驗累計超100億字,我們始終不忘初心,致力于打造中國領先的醫學翻譯品牌,擇一事,終一生,為客戶提供最優質的語言翻譯服務。